서론
경동맥 스텐트 삽입술은 증상성 경동맥 협착 환자의 허혈뇌졸중 예방을 위한 효과적인 치료이며, American Heart Association과 European Stroke Organization에서 발표한 최신 진료 지침에 따르면 경동맥 스텐트 삽입술은 환자의 혈관 상태, 의학적 상태 등으로 인하여 경동맥 내막 절제술 시행이 어려운 경우 이를 효과적으로 대체할 수 있다고 보고되고 있다[
1,
2].
급성 심근경색은 널리 알려진 허혈뇌졸중 발생의 고위험인자로서[
3], 급성 심근경색 이후 한 달 이내에 허혈뇌졸중 발생 위험도가 가장 높다고 알려져 있으며[
4], 대부분은 급성 심근경색 이후 발생한 허혈성 심실의 역운동(ventricular dyskinesis)과 연관되어 발생한 혈전이 주된 원인이 되나, 관상동맥 스텐트 삽입술 자체 또한 시술 자체로 허혈뇌졸중 발생 위험도를 높일 수 있다고 알려져 있으며, 급성 심근경색 이후 발생한 뇌경색의 경우 급성 심근경색 단독 발생에 비하여 한 달 이내 높은 사망률을 보인다고 보고되고 있다[
5]. 본 증례는 급성 심근경색 환자에서 관상동맥 스텐트 삽입 이틀 뒤 발생한 급성 뇌경색에 대하여 경동맥 스텐트 삽입 치료 후 발생한 심정지에 대한 증례를 기술하고자 한다.
증례
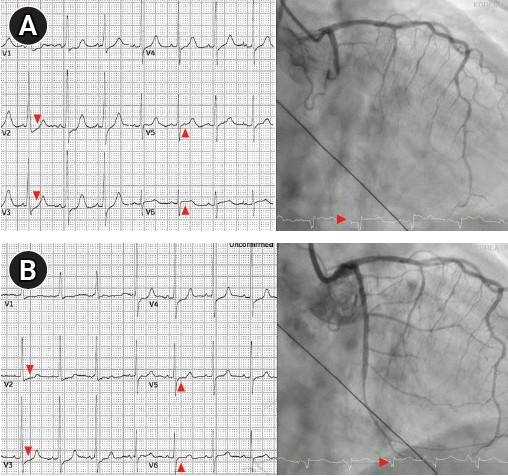
고혈압 및 고지질혈증의 과거력이 있는 70세 남자가 12시간 전 갑자기 발생한 좌측 흉통과 호흡곤란을 주소로 응급실에 내원하였다. 초기 심전도에서 V6 유도의 ST 분절 상승과 V1에서 V4 유도의 ST 분절 하강이 확인되었고, 크레아틴키나아제(creatine kinase)-MB 256 ng/ml, 트로포닌(troponin)-T 2.740 ng/ml, N 말단프로 BNP (N-terminal pro B-type Natriuretic Peptide, NT pro BNP) 1,464 pg/ml로 상승하였다. 이에 급성 하벽 및 후벽 심근경색을 의심하여 관상동맥 조영술을 시행하였으며, 좌측 근위부 좌회선지 동맥(left circumflex artery)의 폐색소견이 확인되어 관상동맥 스텐트 삽입술을 곧바로 시행하여 재관류됨을 확인하였다. 이후 아스피린 100 mg과 프라수그렐(prasugrel) 10 mg을 유지하였다(
Figure 1).
내원 이틀 뒤 환자는 갑자기 우측 상하지의 근력 저하가 Medical Research Council grade 4로 발생하였고, 신경학적 진찰 상 우측 중심성 안면 마비, 구음장애 및 운동 실어증이 확인되어 미국 국립보건원 뇌졸중척도(National Institute of Health stroke scale) 8점으로 확인되었다. 뇌 확산강조영상(diffusion weighted imaged)에서 제한 확산 병변(diffusion restricted lesion)이 양측 전두엽, 좌측 두정엽 및 좌측 측두엽 등 다발 영역에서 관찰되었으나 대부분 좌측 내경동맥 영역에 집중되어 있는 양상으로 확인되었다(
Figure 2). ST 분절 상승 심근경색 환자이나 발생 당일 응급 관상동맥 스텐트 삽입술을 통하여 혈관이 완전히 재개통되었으며, 입원 이후 심근효소의 급격한 감소 추세, 흉통 및 호흡곤란의 회복, 이전 경흉부 심장초음파(transthoracic echocardiography) 상 심근 허혈 소견 외에 구조적 이상 소견 등은 관찰되지 않았음을 고려하여, 조직플라스미노겐활성제(tissue plasminogen activator)를 체중당 0.9 mg (10% bolus over 1 minute, 90% over 60 minutes)의 용량으로 즉각 투여하였으며, 투약 후 신경학적 진찰상 구음장애 및 운동 실어증이 회복되어 뇌졸중척도는 4점으로 호전되었다. 당일 뇌 자기공명혈관조영술(magnetic resonance angiography)을 시행하였으나, 두개 내 동맥의 협착 혹은 폐색은 관찰되지 않았고 근위부 동맥을 평가하기 위해 시행한 대퇴동맥경유뇌혈관조영술(transfemoral cerebral angiography) 상에서 좌측 근위부 내경동맥의 중증도 이상의 협착과 함께 궤양성 죽상경화반이 관찰되었다(
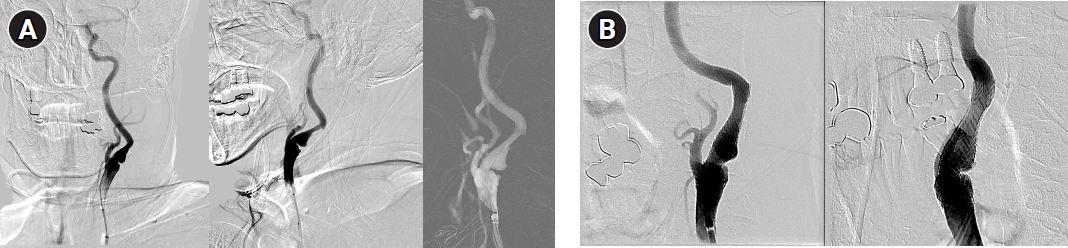
Figure 3).
조직 플라스미노겐활성제 투약 하루 뒤 경흉부 심장초음파를 재시행하였으며 뇌경색 발생 이전에 시행한 검사와 비교하여 심근파열 및 심장압전등의 소견은 관찰되지 않았고, 좌심실 박출률은 일부 호전되었다. 다만 측벽 및 후벽의 수축력의 악화 소견이 관찰되었으나, 이는 새롭게 발견된 심방세동이 원인으로 판단되어 항부정맥 약제(아미오다론, amiodarone)를 투약하였으며, 추적관찰한 심근 효소 수치 또한 전일과 비교하여 크게 감소하였고, 이후 정상범위 내로 유지되었다. 확인된 심방세동에 대하여 환자의 체중 70 kg, 크레아티닌(creatinine) 1.8 mg/dl로, 신사구체 여과율이 38 ml/min임을 고려하여 뇌경색 발생 다음 날부터 에독사반 30 mg을 추가하였으며, 기존에 복용 중이던 프라수그렐 10 mg을 클로피도그렐(clopidogrel) 75 mg으로 변경하고 아스피린(aspirin) 100 mg을 유지 투약 하였으며, 이후 시행한 cytochrome P450 2C19 (CYP2C19) 유전형 검사 상 *1/*1로 이상 소견은 관찰되지 않았다. 환자의 좌측 경동맥의 중증도 이상의 증상성 협착에 대하여, 심근경색 및 뇌경색이 충분히 안정된 것으로 판단하여 뇌졸중 증상 발생 1주일 뒤 balloon dilatation 카테터를 활용한 혈관 성형술(angioplasty) 및 self-expandable open cell 스텐트를 이용한 경동맥 스텐트 삽입술을 시행하였다. 시술 시에 부작용은 없었으며 North American Symptomatic Carotid Endarterectomy Trial 기준 60.2%에서 33.8%으로 협착이 다소 호전되었다(
Figure 3).
환자는 시술 직후 혈역학적으로 안정된 상태였으나, 산소 포화도 및 심전도를 포함한 모니터링 도중 뚜렷한 전조 증상 및 신경학적 변화 없이 갑작스러운 심정지가 시술 4시간 후에 발생하였으며, 심전도에서 무맥성 전기활동(pulseless electrical activity)이 관찰되었다. 곧바로 심폐소생술을 30분 이상 시행했음에도 자발순환회복(return of spontaneous circulation) 없이 심장무수축(asystole) 소견을 보이며 사망하였다. 본 증례보고에 대하여 고려대학교 부속 구로병원 의학연구심의의원회의 승인을 받았다(approval number: 2022GR0304).
고찰
본 증례는 급성 심근경색으로 응급 관상동맥 스텐트 삽입술을 시행한 환자에서 2일 뒤 뇌경색이 발생하여, 이로부터 1주일 이후 증상성 경동맥 협착에 대하여 경동맥 스텐트 삽입술을 시행한 후 4시간 후에 갑작스러운 심정지가 발생하여 사망한 사례이다.
본 증례와 같이 급성 심근경색 이후 응급으로 관상동맥 스텐트 삽입술(non-elective percutaneous coronary intervention)을 시행하고 발생한 뇌졸중 환자의 경우 30일 내 사망률은 20%에 달하며, 뇌경색이 동반되지 않은 환자와 비교하여 30일 내 사망률의 경우 약 3배, 중증도의 심혈관 부작용(major cardiovascular events)의 경우 약 5배의 교차비(odds ratio)를 보인다고 알려져 있다[
5]. 또한 급성 심근경색 환자에서 뇌경색이 동반되지 않은 경우의 1년 내 사망률은 약 20% 가량인 데 비해 뇌경색이 동반된 경우 1년 내 사망률이 30-40%에 달하며 큰 차이를 보인다고 알려져 있다[
6].
급성 심근경색 이후 발생한 뇌경색 환자에서 1개월 내 사망률을 높일 수 있는 요인으로는 고령, 여성, 뇌졸중 과거력, 입원 중 발생한 심인성 쇼크, 입원 중 시행한 기관 삽관 및 기계환기, ST 분절 상승 급성심근경색증(ST-segment elevation myocardial infarction, STEMI) 등이 있으며, 1년 내 사망률을 예측할 수 있는 지표로는 고령, 심부전 과거력, 뇌경색 과거력, 신부전 과거력, 당뇨, 흡연, 입원 기간 중 발생한 심부전, 심방세동 등이 있다고 알려져 있다[
5,
6]. 본 증례의 경우에는 이 중 STEMI 및 심방세동이 확인되었으나 기존 연구에서는 경동맥 스텐트 삽입술이 위험인자로서 보고된 바는 없다.
반면에, 경동맥 스텐트 삽입술(carotid artery stenting) 자체의 경우 시술 후 1개월 내 사망률은 0.7% 정도의 안전한 시술로 알려져 있으며, 경동맥 내막 절제술과 비교하여 뇌경색 발생 위험도는 높으나 심근경색 등 심혈관계 부작용 발생 위험도는 낮은 것으로 알려져 있다[
7]. 경동맥 스텐트 삽입술 후 사망률을 높이는 위험인자로는 여성, 만성 심부전, 뇌졸중 과거력, 당뇨, 시술센터의 적은 시술 경험(1년 내 1-2건 이하) 등이 보고된 바는 있으나[
8], 본 증례의 경우와 같이 최근 경험한 심근경색이 시술 후 사망의 위험인자로 보고된 바는 없다.
경동맥 스텐트 삽입술 과정에서 경동맥굴(carotid sinus)의 압력수용기(baroreceptor)를 자극하면 경동맥굴 신경(carotid sinus nerve)이 활성되어 교감신경이 억제되고 심장으로의 부교감 자극(vagal output)이 촉진되어 시술 중 또는 시술 후 서맥 및 심장무수축이 발생할 수 있다고 널리 알려져 있다[
9]. 일반적으로 서맥 및 심장무수축은 시술 중 ballooning 시에 일시적으로 발생하나[
10], 본 증례에서는 시술 중 및 시술 직후에는 혈역학적으로 안정되었으나 4시간 이후 갑자기 발생하였다는 점에서 차이가 있다. 경동맥 스텐트 삽입술 후 발생하는 심장무수축 환자의 위험인자로는 우측 경동맥 스텐트 삽입술, 시술 반대측 경동맥의 중증도 이상의 협착, 40% 미만의 좌심실 박출률(left ventricular ejection fraction, LVEF) 저하 등이 알려져 있으나[
9], 본 증례에서는 급성 심근경색으로 LVEF가 저하되어 있으나 관상동맥 스텐트 삽입술 전 후 각각 43%와 45%로 확인되어 보고된 명확한 위험인자는 없었다.
급성 심근경색과 동반된 뇌경색 환자의 사망률은 점차 감소하고 있는 추세이나[
6], 본 증례와 같이 급성 심근경색과 이후 발생한 급성 뇌경색 환자의 급성기에 경동맥 스텐트 삽입술을 시행하였을 때 시술 후 심정지 및 사망의 예기치 못한 심각한 합병증이 발생할 수 있음을 경험하여 이를 보고한다.














 PDF Links
PDF Links PubReader
PubReader ePub Link
ePub Link Full text via DOI
Full text via DOI Download Citation
Download Citation Print
Print