노인환자에서 이상지질혈증의 약물치료
Medical treatment of dyslipidemia in the elderly
Article information
Trans Abstract
Worldwide, the proportion of the population aged 65 years or older is rapidly increasing, along with the prevalence of dyslipidemia and cardiovascular disease. Because of decreased physiological functions and comorbidities in the elderly, it is difficult to determine a treatment strategy for each individual. According to the guidelines for dyslipidemia in Europe and the United States, aggressive low-density lipoprotein cholesterol lowering is recommended for secondary prevention of cardiovascular disease as in the younger patient group. Also, newer cholesterol-lowering agents, ezetimibe and PCSK9 inhibitor can be added to achieve treatment goals in high risk groups. However, considering the conflicting study results in primary prevention, it is necessary to fully consider life expectancy and side effects of medications to determine whether to initiate treatment. Several on-going studies are expected to give answers to many complex clinical situations of dyslipidemia treatment in the elderly.
서론
전 세계적으로 65세 이상 인구의 비율은 급격히 증가하고 있으며, 이와 함께 고혈압, 당뇨병, 이상지질혈증과 이로 인한 심뇌혈관질환 유병률도 증가하고 있다. 최근 수십 년간 예방, 조기 진단 및 치료의 현저한 발전에도 불구하고, 여전히 보건의료계와 지역사회에 막대한 사회 경제적 부담을 주고 있다. 우리나라의 경우 65세 이상 인구 비율이 2021년 16.5%에 달하는 고령사회이며, 2026년에는 20%를 넘는 초고령사회로 진입할 것으로 예상된다[1]. 질병관리본부 통계에 따르면, 고혈압 유병률 및 흡연율은 큰 변화를 보이지 않으나, 고콜레스테롤혈증 유병률의 증가가 뚜렷하여, 관상동맥질환 및 뇌혈관질환의 질병부담은 더 커질 것으로 예상된다[2]. 뇌졸중의 경우, 2014년부터 2019년까지 사망률은 12.8%가 감소하였으나, 유병률은 29.7%가 증가하여 의료비용은 지속적으로 증가 추세이다[3,4]. 또한 고령인구의 경우, 여러 동반질환을 함께 가진 경우가 많기 때문에, 이 집단의 지질관리 전략의 중요성은 더 강조되고 있다. 본 종설에서는 노인인구에서의 이상지질혈증의 특징, 약물치료에 대한 최근 진료지침 및 연구동향에 대해 알아보자 한다.
고령인구에서 이상지질혈증의 특징
혈청 지질 농도는 연령에 따라 변화하며, 여성은 폐경 전후로 큰 차이를 보인다. 국민건강영양조사 자료에 따르면[5], 총콜레스테롤은 20세 이후로 증가하여, 남성은 50대, 여성은 60세까지 증가하고 이후 서서히 감소한다[6]. 심뇌혈관질환의 위험도를 낮추는 것으로 알려진 고밀도 콜레스테롤(high-density lipoprotein cholesterol, HDL-C) 농도는 모든 연령층에서 여자가 남자보다 높다. 그러나 60대 이후는 그 차이가 줄어든다. 또한 젊은 성인과 달리 노인에서는 총콜레스테롤, 저밀도 콜레스테롤(low-density lipoprotein cholesterol, LDL-C) 농도, 중성지방 수치가 모두 역전되어 여자가 더 높기 때문에, 고령자, 특히 여성 고령자의 이상지질혈증의 예방과 관리가 더욱 중요해질 것으로 예상되고 있다[7,8].
현재 가이드라인
1. 2018년 미국 심장학회 진료지침
미국 심장학회 진료지침[9]에서는, 죽상동맥경화증성 혈관질환(atherosclerotic cardiovascular disease, ASCVD)이 있는 그룹을 급성 관상동맥 증후군, 심근경색, 협심증, 관상동맥 또는 다른 동맥의 재건술, 뇌경색, 일과성 허혈 발작, 복부대동맥류를 포함한 말초혈관질환으로 정의하고 있으며, 고강도 스타틴 치료로 기준 LDL-C 수치 대비 50% 이하로 낮추도록 하고 있다. 또한 ASCVD가 2개 이상이거나, 하나의 ASCVD와 여러 개의 고위험인자(65세 이상, 가족성 고콜레스테롤 혈증, 관상동맥 우회술이나 스텐트 시술, 당뇨병, 고혈압, 만성신질환, 현재 흡연, 최대 용량 스타틴 치료에도 지속적으로 LDL 100 mg/dl 이상, 울혈성심부전)를 가지는 군은 초고위험군으로 분류하여 최대용량 스타틴 치료에도 지속적으로 LDL-C 70 mg/dl 이상인 경우 에제티마이브를 추가하고, 여전히 지속적으로 70 mg/dl 이상인 경우 proprotein convertase subtilisin/kexin type 9 (PCSK9) 억제제를 추가할 수 있다(Figure 1) [9].
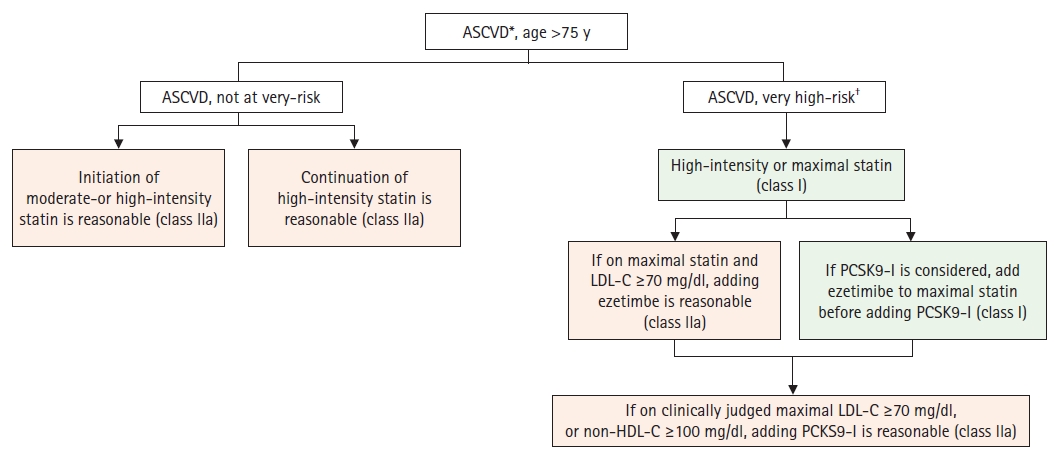
Secondary prevention in the elderly patients with clinical atherosclerotic cardiovascular disease (ASCVD). Adapted from Grundy SM, et al. J Am Coll Cardiol 2019;73:e285-e350, with permission from Elsvier [9]. *Acute coronary syndrome, those with history of MI, stable or unstable angina or coronary other arterial revascularization, stroke, transient ischemic attack (TIA), or peripheral artery disease (PAD) including aortic aneurysm, all of atherosclerotic origin †a history of multiple major ASCVD events or 1 major ASCVD event and multiple high-risk conditions (age ≥65 y, Heterozygous familial hypercholesterolemia, History of prior coronary artery bypass surgery or percutaneous coronary intervention outside of the major ASCVD event(s), diabetes mellitus, hypertension, CKD (eGFR 15-59 ml/min/1.73 m2), current smoking, persistently elevated LDL-C (LDL-C ≥100 mg/dl [≥2.6 mmol/L]) despite maximally tolerated statin therapy and ezetimibe, History of congestive HF).
1차 예방의 경우에서는 LDL-C 190 mg/dl 이상에서는 위험도 평가 없이 고강도 스타틴을 시작하고, 70 mg/dl 이상, 190 mg/dl 미만에서는 심혈관질환 위험도를 공식(pooled cohort equation)으로 따로 계산하여 7.5% 이상인 경우 스타틴 치료를 권장하고 있다. 이를 통한 결정이 확실하지 않은 경우에는 관상동맥석회화 지수(coronary calcium score)를 컴퓨터단층촬영으로 측정하여 score 0을 제외하고는 위험도와 이득을 고려하여 결정하도록 권고하였다. 요약하면, 2차 예방으로는 고강도 스타틴을 일차치료약제로, 목표수치에 도달하지 못할 시 에제티마이브 및 PSCK9 억제제를 고려한다. 1차 예방의 경우 LDL-C 수치 및 여러 위험인자를 고려하여 결정한다.
75세 이상에서는 고강도와 중강도 스타틴을 비교한 임상시험에서는 부작용이 차이를 보이지 않았지만, 고강도 스타틴 부작용(간수치 상승 등), 낮은 순응도, 높은 중단율 등을 보일 가능성이 있기 때문에 중강도 스타틴을 고려해볼 수 있다. 그렇지만 고강도 스타틴을 잘 복용하고 있는 환자에서는 굳이 중단할 필요는 없다고 추천하고 있다. 또한 고강도 스타틴이 중강도 스타틴보다 심혈관계 위험도를 더 낮추는 것으로 나타났는데, 이는 LDL-C 강하효과 차이로 보이며, 따라서 고강도 스타틴의 부작용 혹은 부작용이 걱정되는 상황이라면, 중강도 스타틴과 에제티미브 병용 요법으로 그에 상응하는 효과를 볼 수 있을 것이다.
2. 2019년 유럽 심장학회 진료지침
유럽 가이드라인[10]의 경우 초고위험군, 고위험군, 중등도위험군 및 저위험군으로 분류하여 목표 LDL-C 수치를 명시하고 있다. 위험군 분류에는 ASCVD 및 당뇨병, 고혈압, 만성 신질환 등 위험인자들을 고려한다. 또한, 성별, 연령, 혈압, 흡연 여부에 따른 심혈관계 위험도 차트(Systematic Coronary Risk Estimation chart, SCORE chart)를 사용하여 위험군 분류에 사용하고 있다. ASCVD가 있는 2차 예방이 필요한 경우 초고위험군이며, 목표 LDL-C 수치는 55 mg/dl로, 이전 가이드라인의 70 mg/dl에서 하향 조정되었다. 75세 이상의 경우 2차 예방은 젊은 환자들과 동일하게 치료하며, 1차 예방의 경우에는 개인의 위험도에 따라 스타틴 치료를 고려할 수 있다. 또한, 스타틴 치료를 시작할 때 신장애가 있거나, 약물상호작용이 우려될 때는 저용량으로 시작하여 상향 적정하는 것을 권고하고 있다.
3. 2018년 한국 지질, 동맥경화학회 진료지침
한국 진료지침[11]의 경우 유럽 가이드라인과 마찬가지로 위험인자에 따라 위험군 분류 후 목표 LDL-C 수치를 명시하고 있다. ASCVD 환자는 초고위험군으로 목표 LDL-C 70 mg/dl 미만 혹은 기저치보다 50% 이상 감소시키는 것을 목표로 한다. 유의미한 경동맥 협착 및 복부동맥류, 당뇨병은 고위험군으로 LDL-C 100 mg/dl 이상일 때 치료를 시작한다. 연령, 관상동맥질환 조기 발병의 가족력, 고혈압, 흡연, 저고밀도 콜레스테롤은 주요위험인자로서 2개 이상이면 중등도, 1개 이하이면 저위험군으로 분류하여 생활습관 교정 이후에도 각각 LDL-C 130, 160 mg/dl 이상이면 스타틴 치료를 시작한다(Figure 2) [11]. 또한, 중성지방 500 mg/dl 이상일 때 2차원인을 찾아보고, 지속적으로 높은 경우 췌장염 예방을 위해 fibrate, omega 3 fatty acid를 권고하고 있다. 중성지방 농도가 200-499 mg/dl이면서 LDL-C 농도가 위험군에 따른 목표치보다 낮은 경우 일차적으로 스타틴 치료를 권고하고 추가적으로 fibrate, omega 3 fatty acid를 추가하는 것을 고려할 수 있다.
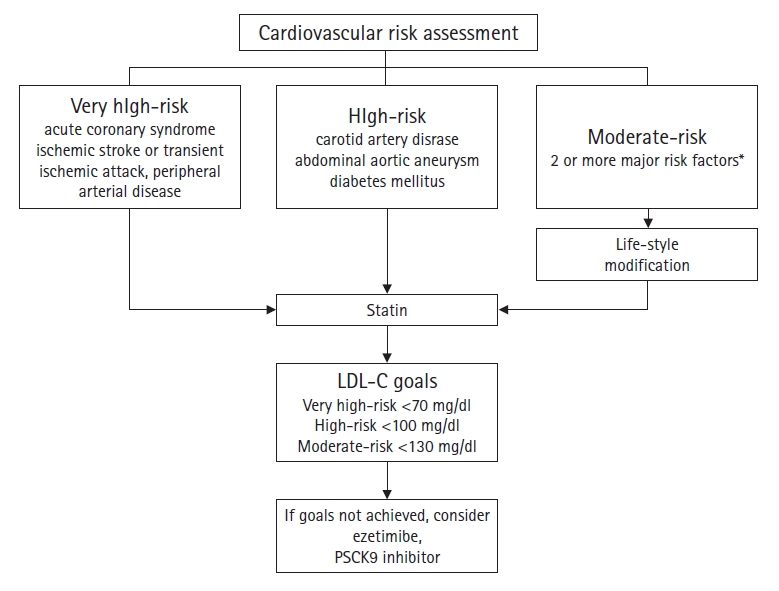
Cardiovascular risk assessment and treatment goals. Adapted from Rhee EJ, et al. J Lipid Atheroscler 2019;8:78–131, according to the Creative Commons license [11]. *Age: male ≥45 years, female ≥55 years, history of early onset cardiovascular disease, hypertension, current smoking, low HDL-cholesterol (<40 mg/dl).
노인에서의 이상지질혈증 치료는 이전 연구결과들을 바탕으로, 1차 예방과 2차 예방에서 모두 젊은 성인과 비교하여 스타틴 사용에 따른 이득은 동일하게 유지되었다. 횡문근융해증이나 간효소 수치 상승과 같은 약물 이상반응도 노인환자에서 유의하게 증가하지는 않아 안전하게 사용할 수 있는 약물이며, 다만 노인환자에서는 동반질환이나 다수의 타 약제를 복용하는 경우가 많으므로 약물 상호작용과 스타틴의 부작용에 보다 주의하여 사용하는 것을 권고하고 있다.
노인에서 지질강하 약물요법의 연구결과
1. 노인에 대한 스타틴 관찰연구
관상동맥 질환 환자에서 스타틴의 효용성은 많은 관찰연구에서 이미 확인되었다. 관상동맥 질환 환자 7,220명 중 80세 이상 655명을 포함한 한 연구에서는 약 3년 동안 추적관찰한 결과, 비교위험도가 0.5 (95% 신뢰구간, 0.26-0.96)로 사망률 감소를 보여주었다[12]. 이 연구의 제한점은 스타틴 치료를 시행한 군과 대조군 간의 위험인자 분포가 고르지 않다는 것이다. 캐나다의 한 코호트 연구에서는 허혈성 심질환으로 입원한 65세 이상의 환자 4,232명을 대상으로 스타틴 사용에 따른 사망률 및 의료기관 이용률에 차이가 있는지 확인하였다[13]. 이 연구에서 스타틴 사용군은 26%의 사망률 감소를 보였으나, 재입원, 외래 진료, 관상동맥 재개통술 비율 등 이후의 의료서비스 이용률에서는 차이를 보이지 못했다. 65세 이상의 요양시설에 입원한 심혈관계 질환을 가진 환자들을 대상으로 한 연구에서는 1년 추적관찰 이후 31%의 사망률 감소를 보였으며, 85세 이상의 코호트에서도 28%의 사망률 감소를 확인하였다. 그러나 재입원율 및 일상생활 능력(activities of daily living) 측정에서는 차이를 보이지 못했다. 언급한 연구들과 다르게, 80세 이상에서 스타틴 치료의 효용성을 입증하지 못한 연구결과들도 있다. 65,000명의 급성 심근경색 생존 환자들에서는 80세 이하에서만 유의한 사망률 감소를 보여주었다[14]. 또한, 12,156명의 영국 급성심근경색 환자 코호트에서는 60-79세의 환자들에서만 심근경색 재발률을 유의하게 낮춰주었고, 80세 이상군에서는 유의한 차이를 보여주지 못하였다[15].
고령의 환자에 대한 1차 예방에 대한 관찰연구에서는 엇갈린 결과들을 보여주었다. 75세 이상 미국인 30만 명을 대상으로 한 연구에서 스타틴은 총 사망률 및 심혈관계 질환 사망률을 각각 25%, 20% 유의하게 감소시켰다[16]. 반면, 46,864명의 스페인 코호트 연구에서는 75세 이상이면서 당뇨병이 없는 환자에서 심혈관계 사건이나 총 사망률을 감소시키지 못하였다[17]. 이 연구에서 7,780명은 2형 당뇨병 환자였으며, 75-84세 당뇨환자에서는 심혈관계 질환 발생률을 24%, 총 사망률을 16% 낮춰주었다. 그러나 85세 이상에서는 스타틴의 효용을 증명하지 못하였으며, 88세 이상에서는 사망률 증가의 경향을 오히려 보여주었다.
이처럼 스타틴 관찰연구에서 80세 이상의 환자군은 스타틴의 효용성에 대해 상반된 연구결과들이 공존하고 있다. 특히, 의료서비스 이용률이나 일상생활 유지능력에서 효과를 보이지 못했다는 점은 노인에서 스타틴 치료 효과를 고려할 때, 다른 동반질환이나 신체적 노쇠화와 같은 인자들을 충분히 고려해야 함을 시사하고 있다.
2. 노인에 대한 스타틴 임상시험
2019년에 발표된 28개의 무작위 배정 임상시험에 대한 메타연구에서는 총 186,854명의 환자 중 14,483 (8%)의 75세 이상의 환자들이 포함되었다. 이 연구에서 75세 이상 환자군에서 1 mmol/L의 LDL-C 감소 시 주요 심혈관계 사건 발생률은 비교위험도 0.87 (95% 신뢰구간, 0.77-0.99)로 감소하는 것이 확인되었다[18]. 다만 이 메타연구에서는 5개의 심부전 및 말기신질환 환자들에 대한 연구도 포함되어 있었으며, 이 연구들은 모두 스타틴 효용성을 보여주지 못한 결과를 보고하기도 하였다[19–23]. 한편, 이 연구에서는 나이에 따른 환자 분류뿐 아니라, 심혈관계 질환 과거력에 따라 환자군을 나눠 분석하였는데, 75세 이상 심혈관계 질환자에서는 비교위험도 0.85로 유의한 심혈관계 사건 감소를 보였으나, 과거력이 없는 70세 이상의 환자에서는 유의한 결과를 보이지 못하였다. 이는 70세 이상의 심혈관계 과거력 없는 환자에서 주요 심혈관계 사건수가 부족하기 때문에 분석에서 충분히 유의한 결과를 도출하지 못한 것으로 설명하고 있으며, 70세 이상의 1차 예방에 대해서는 증거가 부족하다고 볼 수 있다. 노인의 1차 예방의 경우 심혈관계 위험도에 대한 예방효과가 기대여명이나 스타틴의 위험성을 상쇄시키면서 이득을 볼 수 있는지가 중요하다. 현재 노인환자에서 심혈관계 위험도 평가에 대한 세밀한 연구는 부족한 실정이다. 따라서 국내에서도 향후 주요한 코호트 연구를 통해서 고령의 환자에서 각각의 고지혈증 수치에 따른 심뇌혈관질환 발생의 위험도에 대한 평가에 의해 스타틴 투약의 강도 및 용량이 결정될 수 있는 향후에 연구가 필요하겠다.
3. 부작용의 위험
스타틴 사용 중 가장 흔히 보고하는 부작용은 근육통이며[24], 근육 효소(creatinine kinase) 상승을 동반하는 근육병증 및 횡문근융해증 등은 많은 임상의사들이 노인환자에서의 스타틴 사용시 1차적으로 고려하는 부작용이다. 관찰연구를 종합한 메타연구 결과에서는 스타틴 사용군에서 근육병증이 유의하게 더 많이 발생하는 것으로 나타났으나[25], 임상시험에서는 근거가 없는 것으로 정리되고 있다. 최근 미국 심장학회에서 발표된 스타틴 부작용에 대한 종설에 따르면[26], 65세 이상의 참가자를 포함한 대규모 무작위 배정 임상시험들의 결과를 종합해볼 때, 노인인구에서 특별히 근육병증이 더 많이 발생한다는 증거는 없다는 결론이다. 그러나 근육병증 및 횡문근융해증이 보고된 케이스 수 자체가 적어 통계적 유의성을 가지지 못했을 가능성을 고려해야 하며, 임상시험 참가자와 실제 임상에서 마주치는 각각의 환자들은 다르다는 사실을 인지해야 한다. 노인환자에서 낮은 사구체 여과율 및 덜 효과적인 간대사, 그리고 동반질환으로 인한 약물 상호작용 등은 스타틴 치료에 앞서 항상 고려해야할 점이다. 또한, 낮은 체질량지수, 갑상선저하증, 이전 근육병증의 과거력도 위험인자로 보고되고 있어[27], 스타틴 처방에 주의를 기울여야 한다.
2019년 유럽 심장학회 진료지침에 따르면[10], 일반적인 70세 이상 환자에서 여러 스타틴 중 로수바스타틴만 개시용량을 5 mg으로 감량해서 시작할 것을 권고하고 있다. 그러나 신장애나 약물상호작용 위험이 있는 경우 다른 스타틴도 저용량으로 시작하여, 점진적 증량하는 것을 안전한 선택지로 언급하고 있다. 또한, 약물상호작용에 대해서는, 일부 스타틴을 제외하고는 시토크롬 P450 3A4로 가장 많이 대사되기 때문에, 주의해야할 약물을 명시하고 있다(Table 1) [10].
스타틴이 당뇨발생을 증가시킨다는 우려는 JUPITER 임상시험에서 스타틴 치료군에서 당뇨발생이 25% 증가했다는 데이터로부터 시작되었다[28], 이후 5개의 임상시험 데이터를 종합한 메타연구에서 중강도 스타틴에서 위험비율 1.1, 고강도 스타틴에서 1.2로 당뇨발생을 증가시킨다는 결과가 확인되었으나, 이는 이미 당뇨발생의 여러 위험인자들을 가진 환자들에 국한되었다는 분석이다[29]. 또한, 당뇨환자에서 스타틴이 당화혈색소 수치를 거의 증가시키지 않으며[30], 심혈관계 위험도가 높은 환자군임을 고려할 때, 스타틴의 이득이 이런 부작용 위험을 상회한다고 볼 수 있다.
노인환자에서는 치료 개시 여부를 결정하는 것도 중요하지만 부작용에 대한 모니터링이 중요하다. 2018 한국 지질, 동맥경화학회 진료지침에서는 치료 시작 전 알라닌아미노전달효소(alanine aminotransferase) 농도 및 근육 효소를 측정하여 정상치의 3배 이상이면 스타틴 치료를 시작하지 말고 원인에 대한 평가와 치료를 먼저 시행하도록 권고하고 있다. 또한, 치료 후 4-12주 후 2회 이상 연속 측정한 LDL-C 농도가 40 mg/dl 이하라면 스타틴 감량을 고려하며, 이후 3-12개월마다 반복하여 스타틴 효과 및 간 독성 여부를 확인하도록 권고하고 있다. 스타틴 중단 시 1차 예방[31] 및 2차 예방[32]에서 모두 심혈관계 위험도가 중가한다는 연구결과들이 있기 때문에 스타틴 부작용 발생 시 용량 조절 및 다른 종류의 스타틴으로 바꾸는 등의 치료전략이 필요하다.
4. 에제티마이브
소장의 콜레스테롤 흡수를 방해하는 약물로서, 여러 임상시험에서 단독 혹은 스타틴과의 병용 요법으로 추가적인 LDL-C 수치 저하 및 심혈관계 이득을 검증했다. 노인환자군에서는 2015년 IMPROVE-IT 임상시험 결과에서 효능을 입증하였다[33]. 18,144명의 관상동맥질환 환자들은 7년간 추적관찰하여 심바스타틴 40 mg 단독군에 비해 심바스타틴 40 mg과 에제티마이브 10 mg 병용 요법에서 6.4%의 추가적인 심혈관계 위험도 감소를 보였다. 2,798명의 75세 이상 환자들에 대한 하부연구에서는[34], 20%의 추가적인 심혈관계 위험도 감소를 보이면서 부작용에서는 차이가 없어, 고위험군의 노인환자에서는 에제티마이브 병용으로 적극적으로 콜레스테롤을 낮추는 것이 유리함을 입증하였다.
1차 예방에 대해서도 긍정적인 임상시험 결과가 도출되었다. EWTOPIA 75 연구에서는 75세 이상 관상동맥질환의 과거력이 없는 3,411명의 참가자를 에제티마이브 10 mg 단독 치료 및 대조군으로 나누어 4.1년간 추적관찰 하였으며, 비교위험도 0.66으로 주요 심혈관계 사건을 감소시켰다[35]. 아직 1차 예방에서의 에제티마이브의 사용을 가이드라인에서 명시하고 있지 않으나, 노인에서 콜레스테롤의 장 흡수율이 증가함을 고려할 때, 추후 연구결과들을 통해 적응증의 확대가 기대되는 약물이다.
5. PCSK9 억제제(evolocumab and alirocumab)
PCSK9 억제제는 가장 강력한 종류의 콜레스테롤 저하제로 부상했다. 단일클론항체로서 PCSK9에 결합하여 LDL 수용체의 분해를 막아 혈중 LDL-C 농도를 낮추는 약물이며, 2주 또는 4주마다 피하 주사로 투여된다. Evolocumab의 효용성을 검증한 FOURIER 임상시험은 LDL-C 70 mg/dl 이상의 ASCVD 환자들을 대상으로 하였으며, 최대 스타틴 치료에 evolocumab을 추가 투여한 군에서 주요 심혈관 사건의 위험도를 15% 감소시켜 주었다[36]. 이 연구에서는 85세까지의 환자들을 포함하였는데, 참가자들을 4개의 연령 그룹으로 분류한 하부연구에서는 69세 이상의 환자군을 포함한 모든 연령 그룹에서 비슷한 주요 심혈관계 사건의 감소효과를 보여주었다[37].
ODYSSEY OUTCOMES 연구에서는 고용량 스타틴 치료를 시행한 ASCVD 환자에서 Alirocumab을 추가로 투여하였으며, 주요 심혈관사건의 위험도를 15% 추가적으로 감소시키는 결과를 보여주었다[38]. 연령 그룹으로 분석한 하부연구에서는 65세 이상 그룹에서 65세 미만 그룹보다 주요 심혈관계 위험도를 더 감소시켜주는 것으로 나타났다(위험비율, 0.78 대 0.89) [39]. 또한, 75세 기준으로 두 그룹으로 나눴을 때는 위험비율의 차이는 보이지 않았으며, 위약군에 비해 alirocumab군에서 부작용은 더 증가하지 않았다. 두 연구에서 심혈관질환의 초고위험군은 LDL-C를 기존수치보다 낮추는 것이 부가적으로 도움이 되며, PCSK9의 안정성을 입증하였고, 미국과 유럽 주요 가이드라인에 이점이 반영되었다.
진행 중인 연구들
1. Low- and Moderate-intensity Statin and Clinical Outcome of Primary Prevention in Individuals Aged >75 Years (SCOPE-75 RCT STUDY, NCT03770312)
국내 다기관, 개방형, 무작위 배정 임상시험으로 심혈관 질환 1차 예방에서 저강도와 중강도 스타틴의 효용성 및 안정성을 비교하는 연구이다. 이 연구에서는 76-85세 사이의 고령환자들이 포함될 것이며, LDL-C 160-189 mg/dl이면서 심혈관계 과거력이 없거나, LDL-C 80-159 mg/dl이면서, 하나이상의 심혈관계 위험인자(남자, 당뇨, 고혈압, 흡연, HDL-C 40 mg/dl 미만, 조기 심혈관질환 발생의 가족력)를 가진 환자들을 대상으로 한다. 6년간 추적관찰하며, 1차 결과는 스타틴 관련 근육증상(statin associated muscle symptoms), 2차 결과는 심혈관계 질환 사망률, 심근경색, 뇌졸중, 관상동맥 중재술 및 불안정 협심증으로 인한 입원이다. 국내 연구로서, 한국인에서의 1차 예방의 효용성 및 안전성에 대한 증거를 제공할 수 있을 것으로 기대하고 있다.
2. Statins In The Elderly (SITE, NCT02547883)
프랑스 단일기관, 개방형, 무작위 배정 임상시험으로, 스타틴 중단에 따른 사망률 및 질보정생존연수(quality-adjusted life year)를 평가한다. 75세 이상의 최소 1년 이상 1차 예방으로 스타틴을 처방 받았던 환자들을 대상으로 스타틴 지속군과 중단군으로 나눠 6년간 추적한다. 1차 결과는 획득한 질보정생존연수 대비 비용으로 평가하며, 2차 결과는 삶의 질 및 심혈관계질환, 당뇨, 인지저하 사건 발생률이다. 프랑스의 경우 스타틴으로 인한 건강보험공단 지출이 75세 이상에서 매년 200만 유로에 달하기 때문에, 1차 예방 중단에 대한 근거를 제공하는 목적으로 시작된 연구이다. 노인환자에서는 임상적 지표뿐만 아니라, 기대여명과 삶의 질이 중요하여, 이에 대한 비용효율적 측면에 답을 제시할 수 있을 것으로 기대된다.
3. A Clinical Trial of STAtin Therapy for Reducing Events in the Elderly (STAREE, NCT02099123)
호주 다기관, 무작위 배정 임상시험으로, 70세 이상의 독립적 생활이 가능하며, ASCVD이나 치매, 혹은 당뇨를 가지지 않은 참가자를 대상으로 한다. 8년간 atorvastatin 40mg 과 위약군으로 나누어 추적관찰하며, 1차 결과는 사망률, 치매 및 일상생활 장애 발생률, 주요 심혈관계 사건 발생률이다. 다양한 2차 결과 분석이 계획되었으며, 심혈관계 사망, 심근경색, 입원기간, 당뇨, 암, 인지기능장애 발생, 삶의 질, 스타틴의 비용효율성, 뇌졸중 발생 등이 포함되어 있다. 약 18000명의 목표 참가자수를 가진 큰 연구로서, 고령환자에서 스타틴 사용에 대한 다양한 논의점에 근거를 제시할 수 있을 것으로 기대된다.
4. Pragmatic Evaluation of Events And Benefits of Lipid-lowering in Older Adults (PREVENTABLE, NCT04262206)
미국 다기관, 무작위 배정 임상시험으로, 75세 이상이며, 심혈관계 질환, 장애 및 치매를 가지지 않은 지역사회 거주자를 대상으로 한다. 5년간 atorvastatin 40 mg과 위약군으로 나누어 추적관찰하며, 1차 결과는 치매 및 만성 장애가 없는 환자수를 측정한다. 2차 결과는 심혈관계 사망, 관상동맥질환으로 인한 입원, 심부전, 뇌졸중, 관상동맥 중재술 및 인지기능 장애 발생을 측정한다. STAREE 연구와 마찬가지로, 주요 심혈관계 질환 예방 및 인지기능 장애와 신체장애 발생률에 근거를 제시할 수 있을 것으로 기대된다.
결론
75세 이상의 노인에서는 2차 예방에 비해 특히 1차 예방에 대한 지질강하 약물에 대한 효용성과 안정성에 대한 증거는 상대적으로 부족한 편이다. 임상의사는 노인환자의 신체적 특성, 동반질환, 복용약물 등을 확인후 심혈관계 위험도를 평가하여 개개인에 맞는 지질강하 전략을 세워야 한다.
Notes
Conflicts of Interest
The authors have no potential conflicts of interest to disclose.
Funding
None.

